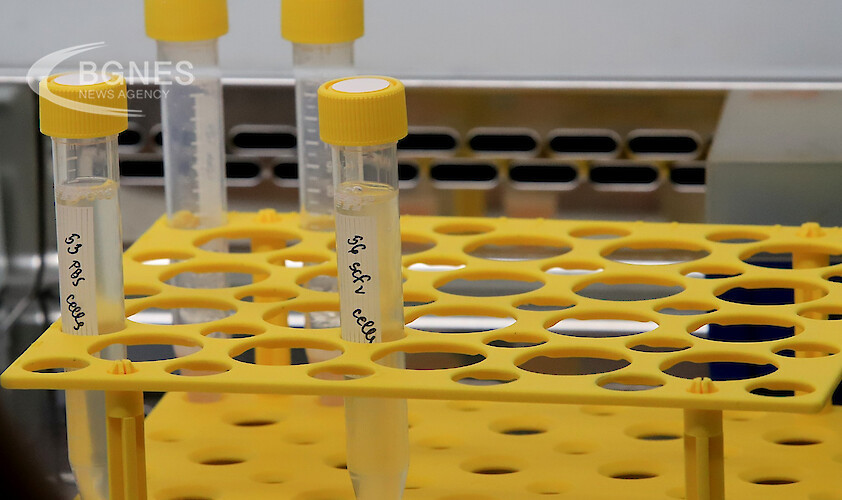
Pfizer/ BioNTech информират за необходимост от трета доза на ваксината
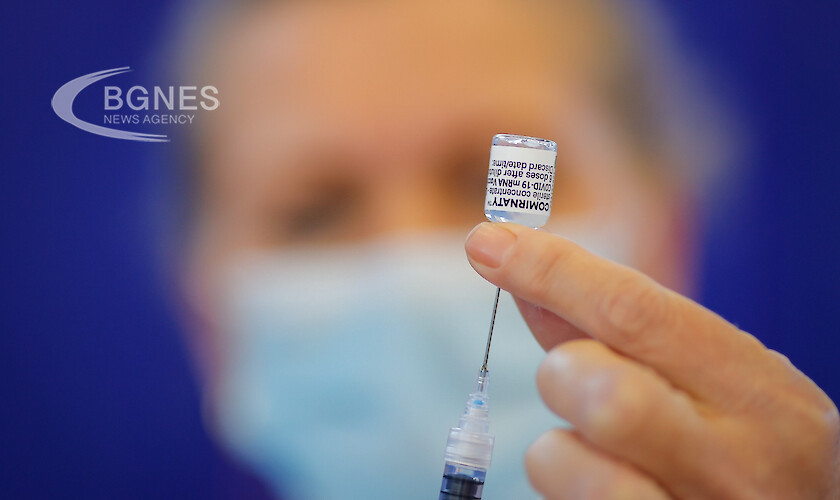
Американската компания Pfizer, която заедно с германския си партньор BioNTech разработи ваксина срещу коронавируса на Comirnaty, възнамерява да информира в близко бъдеще властите на САЩ за необходимостта да се използва трета (бустер) доза. Пише за това с позоваване на източниците си вестник „Вашингтон пост“.
Брифингът може да се състои в понеделник и в него се очаква да вземат участие Антъни Фаучи, директор на Националния институт по алергични и инфекциозни болести в САЩ, Франсис Колинс, ръководител на Националните здравни институти в САЩ, Рошел Валенски, ръководител на Американските центрове за контрол и превенция на заболяванията (CDC) и изпълняващата длъжността директор на Управлението по въпросите на качеството на лекарствата и храните на САЩ (FDA) Джанет Уудкок.
В четвъртък Pfizer и BioNTech обявиха плановете си да предоставят данни за пробни дози на FDA и Европейската агенция по лекарствата (EMA) през следващите седмици. Както се отбелязва в доклада, „първоначалните резултати от проучването показват, че бустерната доза, приложена шест месеца след втората доза, има стабилен профил на толерантност, предизвиквайки високи титри на антитела, които са 5-10 пъти по-високи, отколкото след две първични инжекции".
Тъй като на свой ред, малко след публикуването на прессъобщението, Pfizer и BioNTech информираха „Ройтерс“, FDA и CDC заявиха в съвместно изявление, че според тях американците, завършили курс на ваксинация срещу коронавирус, понастоящем не се нуждаят от трета доза от лекарството. "Ще бъдем готови за бустер дози, ако и когато науката покаже, че е това е необходимо", казаха те ./БГНЕС